哪些PET生物标记物对追踪HD疾病进展最有效?
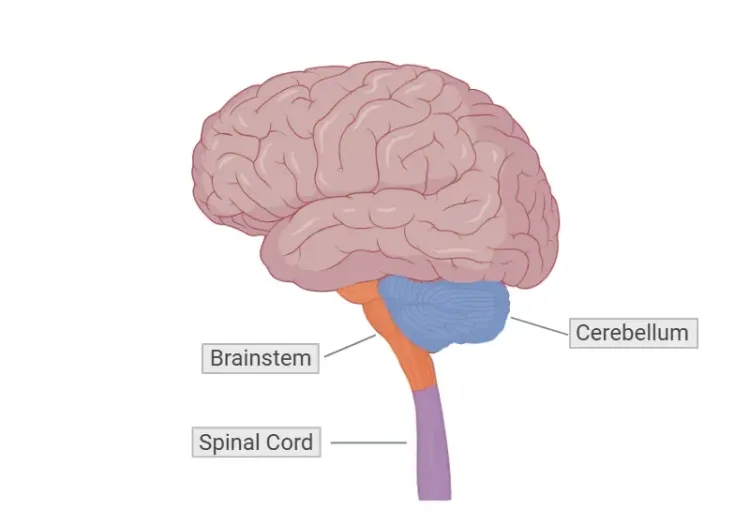
亨廷顿氏病
亨廷顿氏病(HD)是一种罕见的、进行性的神经退行性疾病,以常染色体显性遗传方式遗传。症状通常在35至40岁之间出现,但在极少数情况下,青少年型亨廷顿氏病(JHD)可在20岁之前出现(Klöppel, 2009)。该病的特征是运动功能、认知能力和神经精神健康逐渐衰退。HD的潜在病因是HTT基因突变,其中CAG重复序列的扩张导致产生有毒的突变亨廷顿蛋白(mHTT)。当CAG重复序列计数超过39时,疾病就会显现,重复序列计数越高,发病越早,病情进展越快(Reiner,2011 ;Wijeratne,2021)。
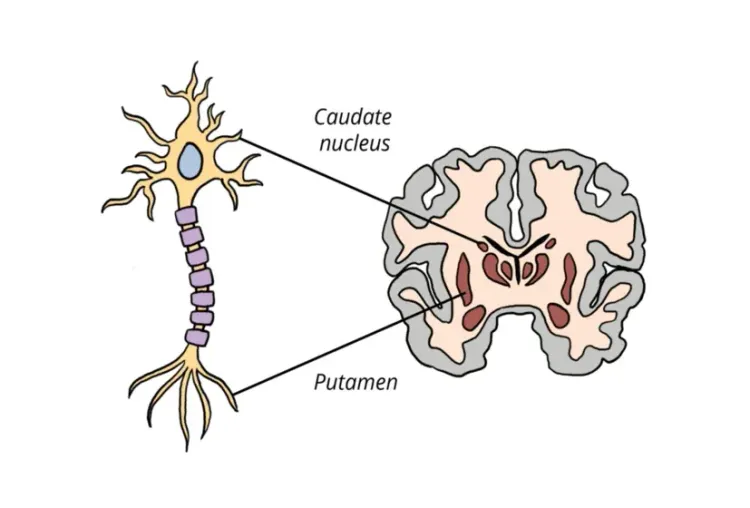
HD的一个关键病理特征是纹状体中多刺神经元(MSNs)的变性,并伴有结构变化,如纹状体萎缩。神经影像学,特别是磁共振成像(MRI)和正电子发射断层扫描(PET)扫描,可以检测到早期脑部变化,通常在运动症状出现之前,为疾病的进展和早期干预的潜在途径提供了至关重要的见解(Klöppel,2009 ;Hobbs,2024)。
尽管目前尚无疾病改良疗法,但正在进行的研究专注于靶向mHTT聚集物,该聚集物在疾病的病理学中起着核心作用。PET成像通过可视化大脑中的各种分子和代谢变化,有助于监测疾病进展。这些变化包括葡萄糖代谢、多巴胺能活性、磷酸二酯酶水平和神经炎症的改变(Cybulska,2020)。此外,旨在定量和追踪mHTT聚合物的全新PET放射性配体正在研发中,有望成为评估新疗法疗效的有用工具(Fazio,2018 ;Cybulska,2020 ;Dickmann,2024)。
大脑葡萄糖代谢
纹状体代谢低下是HD的最早生物标志物之一,可通过[18F]氟代脱氧葡萄糖(FDG)PET成像检测。这种代谢下降通常在临床症状出现之前发生。纵向研究表明,大脑皮层下和皮层区域的葡萄糖代谢都会逐渐下降,包括纹状体、丘脑、岛叶、后扣带回、前额叶皮层和枕叶皮层(Fazio,2018)。此外,皮层葡萄糖代谢的减少与认知缺陷的恶化有关(Fazio,2018)。
在JHD中,纹状体和嗅皮质中的FDG摄取量低于成人HD。相反,成人HD患者的皮质区域(如左下顶叶回和左扣带回)的减少更为明显(Caligiuri,2024)。纵向研究还揭示了不同的代谢下降模式,成人型HD的皮质FDG摄取量下降更为一致,而JHD则表现出更大的差异(Caligiuri,2024)。有趣的是,PET研究已经确定了HD基因携带者早期丘脑代谢亢进,一旦临床症状出现,代谢亢进就会减少(Feigin,2007)。这种丘脑早期代谢亢进可能反映了代偿机制,但其确切作用尚不清楚(Feigin,2007 ;Hellem,2021)。
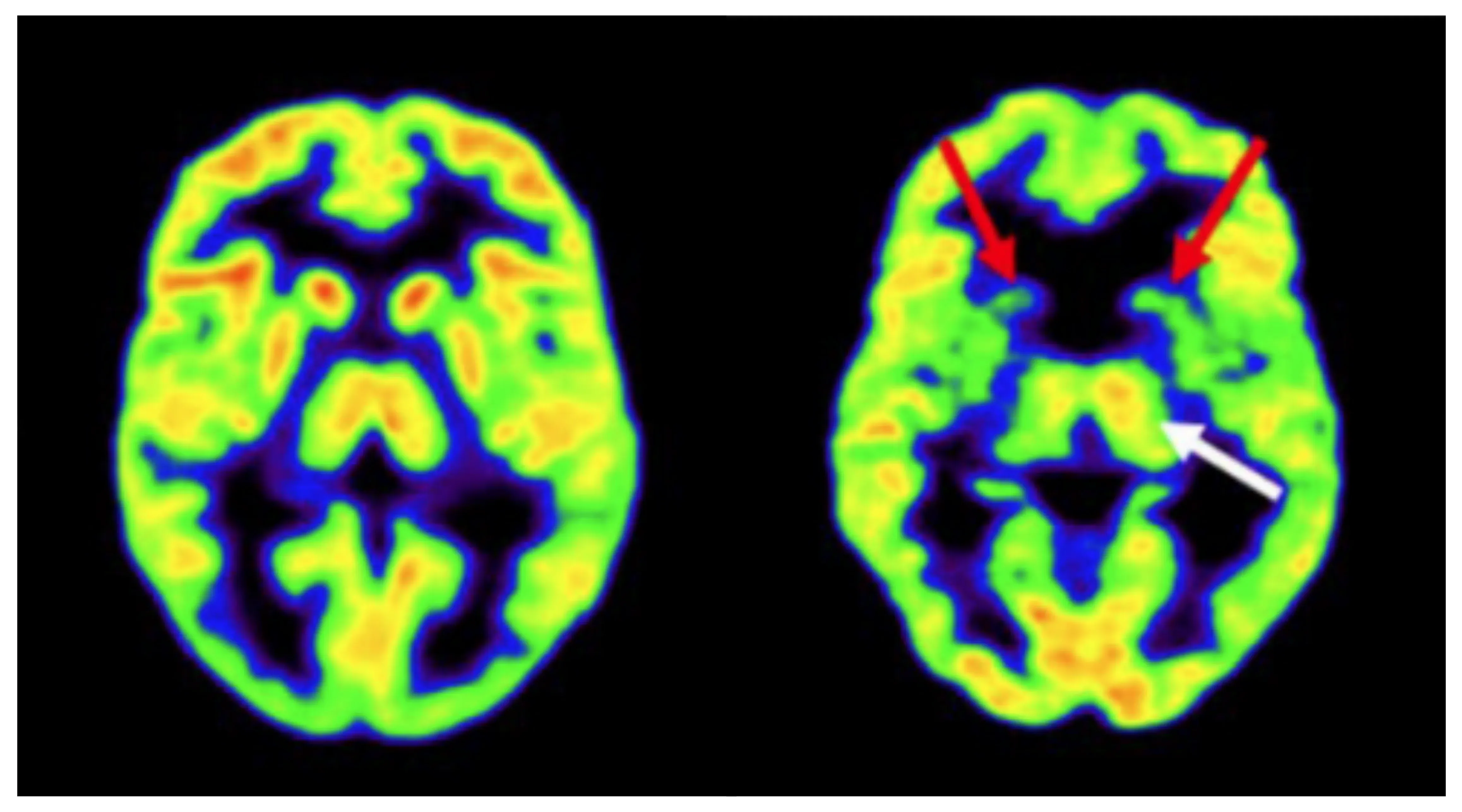
FDG PET扫描显示健康对照组(左)和HD基因扩增携带者(右)的显像。HD基因扩增携带者显示双侧纹状体代谢降低(红色箭头),左丘脑代谢可能出现代偿性增加(白色箭头)。图片改编自Hellem等人(Hellem,2021)在知识共享署名许可协议下的作品。
多巴胺能成像标记物
纹状体中多巴胺能神经元的退化是HD的典型特征,会导致多巴胺受体活性失调。使用针对多巴胺D1和D2/3受体的示踪剂进行PET成像,有助于深入了解疾病的发展过程。例如,使用[11C]SCH-23390示踪剂的研究表明,显性HD患者的纹状体D1受体密度明显降低,与健康对照组相比降低了约50%(Cybulska,2020)。纵向研究表明,显性HD患者的D1受体损失更缓慢,年下降率为2%,而隐性HD患者的年下降率为5%(Cybulska,2020)。
同样,使用[11C]raclopride(一种用于量化D2/3受体的PET示踪剂)进行的PET成像显示,纹状体中的D2受体损失非常明显,且随疾病阶段而变化,前驱HD的损失率为10-50%,而显性HD的损失率为40-60%(Fazio,2018)。此外,在显性HD中,大脑皮层中D2/3结合的减少与神经心理学测试中较差的表现相关,特别是那些评估语言流畅性和记忆力的测试(Cybulska,2020)。
使用突触前标记物(如[11C]二氢四苯嗪(DTBZ))的PET成像研究显示,显性HD患者的纹状体中囊泡单胺转运体2(VMAT2)结合减少。此外,[11C]β-CIT PET扫描显示纹状体中的多巴胺转运蛋白(DAT)结合减少了50%,进一步证实了多巴胺能功能障碍在HD病理中的作用(Fazio,2018)。
磷酸二酯酶10A(PDE10A)成像
PDE10A是一种在MSNs中高度表达的酶,可通过PET成像与配体(如[18F]JNJ42249152、[18F]MNI-659和[11C]IMA-107)进行监测(Fazio,2018)。在显性HD中,PET成像显示纹状体结合显著减少,这与疾病严重程度相关(Cybulska,2020)。纵向研究表明,与健康对照组相比,这种减少在纹状体、尾状核和苍白球中更为明显,年下降率更高(Cybulska,2020)。
有趣的是,在HD前期,运动丘脑核的结合度增加,表明随着症状的出现,补偿性反应会减弱(Cybulska,2020)。这些PDE10A的早期改变可以在临床症状出现前25年检测到,并可能作为疾病发作的预测生物标志物,为干预提供潜在靶点 (Niccolini, 2015)。
神经炎症标记物
神经炎症是亨廷顿舞蹈症的另一个特征,小胶质细胞活化是主要指标。使用针对18-kDa转运蛋白(TSPO)的示踪剂(如[11C]PK11195)进行的PET成像显示,在HD的显性和隐性阶段,放射性配体的结合均增加,表明早期小胶质细胞活化是疾病的潜在生物标志物(Cybulska,2020)。在包括纹状体、皮层、苍白球和岛叶在内的多个大脑区域中观察到了结合力的增强,这些区域与运动、认知和精神功能有关(Cybulska,2020)。这种神经炎症标记物可能有助于在针对疾病改良疗法的临床试验中对患者进行分层,从而有可能帮助早期识别有症状转换风险的患者(Hobbs,2024)。
总体而言,HD是一种复杂的神经退行性疾病,神经影像学的进步大大加深了我们对疾病早期进展的理解。PET成像揭示了与葡萄糖代谢、多巴胺能活性、磷酸二酯酶表达和神经炎症相关的关键生物标志物。这些发现不仅有助于追踪疾病进展,还为治疗干预提供了潜在靶点。
HD中PET成像生物标记与传统的临床结果测量有何关联?
PET成像为追踪HD早期疾病进展提供了有力工具,并与临床结果测量密切相关。例如,显性HD前期FDG PET成像显示纹状体代谢与CAG和年龄乘积(CAP)评分之间存在很强的负相关性。这一观察结果表明,随着个体接近运动症状的发作,纹状体的代谢活动会减少(Hellem,2021)。有趣的是,纹状体的新陈代谢比核磁共振成像体积测量更能解释CAP评分的变化,这凸显了PET在早期追踪疾病进展的敏感性(Hellem,2021)。
除了纹状体变化外,显性前期的皮质代谢逐渐减低与认知缺陷的进展有关(Fazio,2018)。显性前期携带者的尾状核和壳核代谢减低与症状转换的风险增加有关(Hobbs,2024)。横断面数据还表明,在预显性携带者中,基底神经节代谢不足与精神运动速度减慢之间存在关联(Hobbs,2024)。在显性HD中,纹状体和皮质代谢不足与功能能力、运动功能、语言学习、记忆和整体认知障碍有关(Hobbs,2024)。此外,在预显性和显性阶段,皮质代谢不足都与算术题解题困难有关,而早期显性HD中皮质和边缘代谢网络的变化与冷漠有关。
在JHD中,葡萄糖代谢的年度变化越大,肌张力障碍、帕金森症和独立性降低就越严重(Caligiuri,2024)。PET成像研究还表明,在HD前期,纹状体D2受体结合减少与执行功能障碍和语言流畅性降低有关,而在HD前期和HD期,PDE10A结合丧失与运动障碍有关(Hobbs,2024)。
PET成像在高清临床试验中的未来发展方向是什么?
高清研究领域最有前景的未来发展方向之一是开发能够与mHTT聚集体特异性结合的PET放射性配体。这些放射性配体在旨在降低mHTT水平的临床试验中可以发挥关键作用,使研究人员能够可视化并量化大脑靶点的结合,从而深入了解区域分布(Lieberman,2022 ;Hobbs,2024)。然而,与其他神经退行性疾病(如阿尔茨海默病(AD)和帕金森病(PD))中的错误折叠蛋白相比,mHTT聚合物的丰度相对较低,这给研究带来了挑战(Dickmann,2024)。为了解决这个问题,必须开发对mHTT具有高度选择性、而对TDP-43、α-突触核蛋白、tau蛋白和淀粉样β蛋白等其他蛋白聚集物具有高度选择性的高亲和力配体(Dickmann,2024)。
已经对几种有前景的PET配体进行了测试,以确定它们是否能够靶向mHTT,包括[11C]CHDI-180R、[11C]CHDI-626、[18F]1和[18F]CHDI-650。尽管这些配体具有潜力,但其中许多对mHTT的选择性和亲和力有限,有些甚至因疗效不佳而停用(Dickmann,2024)。为了解决这个问题,研究人员继续专注于设计和评估新型PET放射性配体,这些配体能够可靠地靶向体内mHTT(NCT06634628)。这些放射性配体的成功开发将为检测和监测mHTT聚集体提供一种非侵入性的方法,这对于HD的临床试验和早期诊断都是一项重大进展(Kaur,2021)。
此外,这些放射性配体可以为疾病进展提供宝贵的见解,从而在临床试验中实现更精确的患者分层。它们还可以在评估针对mHTT的疾病改良治疗反应方面发挥关键作用,从而提高治疗效果(Kaur,2021)。
在高清晰度下,mHTT蛋白聚集的积累,特别是在纹状体中,会导致神经变性,并伴有运动、认知和神经精神障碍。目前,对mHTT具有高亲和力和选择性的PET放射性配体仍在研发中,但有望实现mHTT在大脑中的客观量化。这些工具可以为追踪疾病进展和评估临床试验中针对mHTT的新疗法提供关键指标,从而推进诊断和治疗策略的发展。
点击复制链接
我们的团队非常乐意回答有关亨廷顿氏病临床试验中PET生物标记物的任何问题,或提供有关我们其他成像服务的具体信息。
相关内容
神经影像学在神经疾病临床试验中的最佳实践的最新信息。
小脑共济失调临床试验和成像生物标记
在脊髓小脑共济失调临床试验中,通过结构核磁共振成像、扩散张量成像和磁共振波谱成像生物标记来监测疾病进展。
亨廷顿病临床试验中的核磁共振成像生物标记物
亨廷顿氏病(HD)临床试验中结构性和弥散性MRI成像生物标志物使用概述。
结节性硬化症(TSC)的神经影像生物标记
脑部结构磁共振成像和弥散加权成像生物标记概述,用于监测TSC临床试验中疾病修正疗法的有效性。
神经疾病中蛋白质折叠异常的建模
神经变性中蛋白质错误折叠机制的计算建模,以及疾病治疗药物的研发与应用。
弗里德雷希运动失调症临床试验的影像生物标记
MRI和DTI成像生物标记在弗里德雷希特共济失调症(FRDA)研究及多中心临床试验中的应用概述。
多系统萎缩(MSA)临床试验中的核磁共振成像(MRI)
该资源概述了在MSA研究中作为生物标志物的容积核磁共振成像和弥散加权成像(DWI)的实用性。