Quelles sont les caractéristiques cliniques et les bases génétiques de la FRDA?
Caractéristiques cliniques
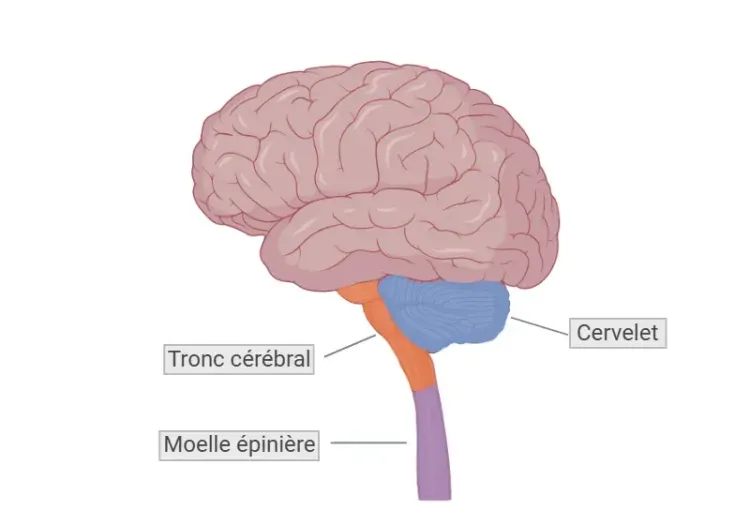
L'ataxie de Friedreich (FRDA) est une maladie neurodégénérative rare, autosomique récessive, caractérisée par une ataxie progressive des membres et de la démarche, affectant principalement la moelle épinière, le cervelet et le tronc cérébral. Le FRDA est l'ataxie autosomique récessive la plus fréquente, avec une prévalence d'environ 1 individu sur 40 000, affectant principalement les descendants d'Europe occidentale et méridionale (Vankan, 2013). La maladie se manifeste généralement pendant l'enfance ou l'adolescence, habituellement entre 10 et 15 ans, bien que certains enfants puissent présenter des symptômes avant l'âge de 10 ans (Bidichandani, 1998; Mahale, 2024). Les formes moins courantes comprennent l'ataxie de Friedreich à début tardif (LOFA), qui se manifeste après l'âge de 25 ans, et l'ataxie de Friedreich à début très tardif (VLOFA), qui apparaît après l'âge de 40 ans (Bidichandani, 1998). Les hommes et les femmes sont également touchés.
Les caractéristiques cliniques du FRDA comprennent une ataxie progressive des membres et de la démarche, une perte de coordination et une dysarthrie, qui sont toutes des symptômes neurologiques impliquant le cerveau et la moelle épinière. D'autres symptômes neurologiques peuvent inclure des mouvements oculaires anormaux, une perte d'audition et des tremblements (Pandolfo, 2009). La scoliose est fréquente, affectant une proportion significative des individus atteints de FRDA, et est considérée comme une manifestation squelettique en raison de son association avec la faiblesse musculaire et l'ataxie. Le diabète, une caractéristique moins courante, se développe souvent en raison d'une atteinte du pancréas (Bidichandani, 1998). L'atteinte cardiaque, en particulier la cardiomyopathie, est une caractéristique grave de la maladie, qui entraîne souvent une mortalité prématurée. L'évolution de la maladie se caractérise par un déclin progressif de la mobilité, la plupart des individus ayant besoin d'une assistance en fauteuil roulant environ 10 ans après l'apparition des symptômes (Pandolfo, 2009).
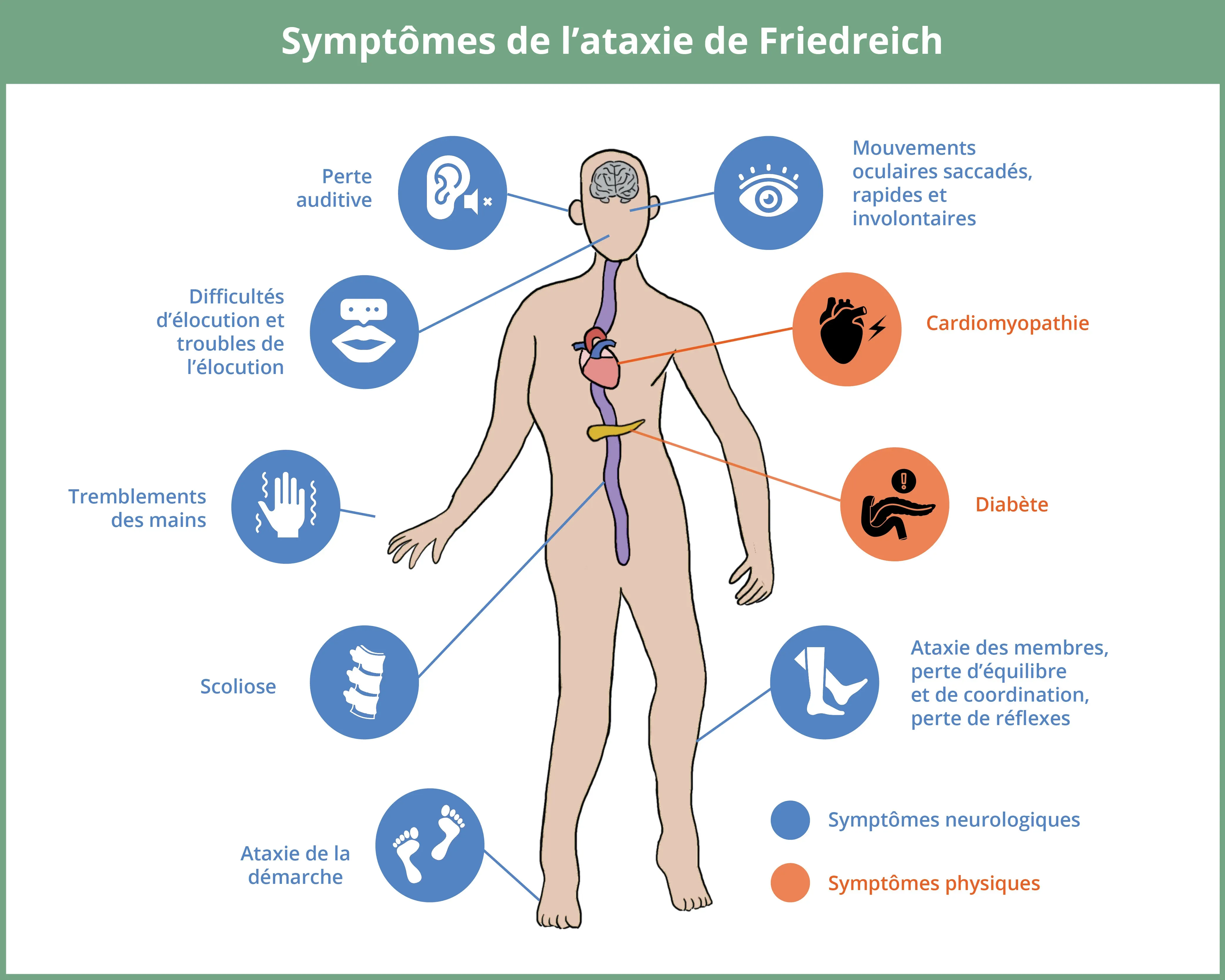
L'ataxie de Friedreich (FRDA) est une maladie neurodégénérative rare qui se manifeste généralement pendant l'enfance ou l'adolescence. Elle affecte principalement la moelle épinière, le cervelet et le tronc cérébral, provoquant une série de symptômes neurologiques et physiques.
Cliquez pour copier le lien
Fondements génétiques
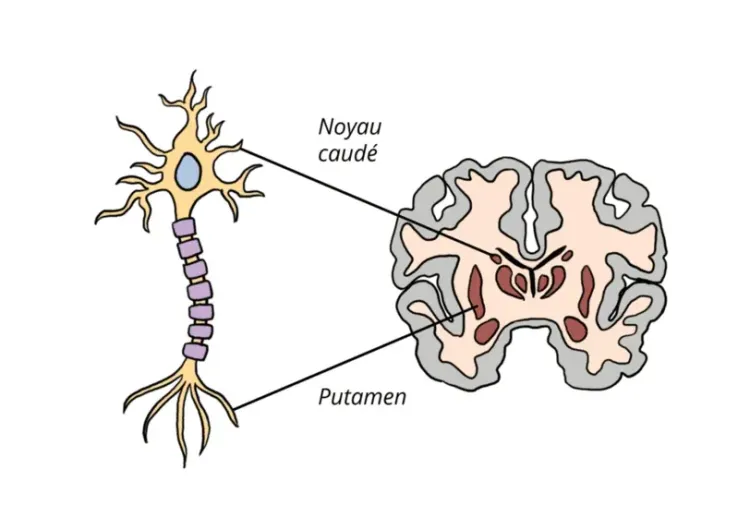
La FRDA est causée par des mutations du gène FXN situé sur le chromosome 9. La mutation la plus fréquente est une expansion de répétitions trinucléotidiques GAA dans l'intron 1 du gène FXN, entraînant une réduction de la production de la protéine frataxine (Koeppen, 2011). La frataxine joue un rôle essentiel dans la fonction mitochondriale, en particulier dans la régulation du fer, et sa déficience entraîne un stress oxydatif et une perturbation du métabolisme cellulaire (Dong, 2024). Environ 96% des cas de FRDA sont dus à des expansions répétitives GAA sur les deux allèles du gène FXN, ce qui entraîne une réduction significative des niveaux de frataxine (Bidichandani, 1998). Les recherches montrent que la longueur de l'expansion répétée GAA est en corrélation avec un âge d'apparition plus précoce et une gravité accrue de la maladie (Pandolfo, 2009; Koeppen, 2011).
Les porteurs hétérozygotes d'une mutation du FXN présentent des niveaux réduits de frataxine mais ne présentent pas de symptômes de FRDA. Dans un sous-ensemble plus restreint de cas (environ 4%), un allèle présente une expansion de la répétition GAA et l'autre allèle porte une mutation différente, telle qu'une délétion ou une mutation ponctuelle (Bidichandani, 1998). Ces cas ont tendance à présenter des symptômes cliniques plus légers que ceux qui présentent deux allèles expansés.
Le diagnostic
Le diagnostic de la FRDA repose principalement sur l'évaluation clinique, qui comprend un examen physique visant à évaluer les signes d'ataxie, les troubles de l'équilibre, la faiblesse musculaire et d'autres déficits neurologiques (Bidichandani, 1998). Les tests génétiques visant à identifier les mutations du gène FXN sont utilisés pour confirmer le diagnostic, tandis que l'échocardiographie permet d'évaluer l'atteinte cardiaque. Les techniques de neuro-imagerie, telles que l'imagerie par résonance magnétique (IRM) du cerveau et de la moelle épinière, sont utilisées pour évaluer les changements structurels (Bidichandani, 1998).
Compte tenu de la gravité et de la complexité des caractéristiques cliniques du FRDA, il est nécessaire de poursuivre les recherches sur les interventions thérapeutiques. Le développement de biomarqueurs fiables pour la détection précoce de la maladie, qui permettrait des interventions opportunes, est tout aussi essentiel. Les progrès des biomarqueurs, y compris des marqueurs d'imagerie, sont également essentiels pour suivre la progression de la maladie et évaluer l'efficacité des traitements thérapeutiques dans les essais cliniques.
Quelles sont les cibles thérapeutiques des essais cliniques actuels sur le FRDA?
Les essais cliniques actuels sur la FRDA se concentrent sur l'amélioration de la fonction mitochondriale, la réduction du stress oxydatif et la modulation des voies métaboliques contrôlées par la frataxine. Les thérapies de remplacement de la frataxine et les approches de remplacement de gènes constituent d'autres domaines clés de recherche.
L'omaveloxolone (SKYCLARYS®), développé par Biogen, est le seul traitement approuvé par la FDA pour le FRDA, ayant reçu l'approbation en février 2023, suivie par l'approbation de la Commission européenne en février 2024 (Pilotto, 2024). Plusieurs autres entreprises et instituts de recherche mènent des essais cliniques pour d'autres thérapies. Notamment, PTC Therapeutics mène un essai de phase 3 sur la vatiquinone (NCT05515536) (Lee, 2024). Un essai de phase 1/2 de l'élamipretide, développé par le Children's Hospital of Philadelphia et Stealth Biotherapeutics, est également en cours (NCT05168774). Le fumarate de diméthyle fait l'objet d'un essai de phase 2 en Italie (EUTC : 2022-503016-16-00). Larimar Therapeutics explore le namlabofusp, une thérapie de remplacement de la frataxine, dans des essais de phase 1 (NCT06681766) et de phase 2 (NCT06447025) (Clayton, 2024). Des thérapies de remplacement génique sont à l'étude, notamment le LX2006 de Lexeo Therapeutics en collaboration avec Weill Cornell, qui fait l'objet d'un essai de phase 1/2 (NCT05445323).
En outre, la Friedreich's Ataxia Research Alliance (FARA) a lancé une importante étude d'histoire naturelle, appelée TRACK-FA (NCT04349514), pour étudier les biomarqueurs de neuro-imagerie dans la FRDA (Georgiou-Karistianis, 2022). L'étude, qui inclut plus de 200 participants FRDA dans sept sites internationaux, utilise l'IRM, l'imagerie du tenseur de diffusion (DTI) et la spectroscopie par résonance magnétique (MRS) pour explorer les changements longitudinaux dans les régions clés d'intérêt, y compris le noyau denté, le cervelet, les pédoncules cérébelleux supérieurs et la moelle épinière, au début de l'étude, à 12 mois et à 24 mois. Les résultats visent à identifier des biomarqueurs d'imagerie capables de suivre la progression de la maladie et de servir de critères d'évaluation fiables dans les essais cliniques.
Quels biomarqueurs IRM et DTI sont efficaces pour détecter et suivre la progression de la maladie dans la FRDA?
Le FRDA affecte principalement le cervelet, la moelle épinière et le tronc cérébral, avec une neuropathologie significative dans le noyau denté, les ganglions de la racine dorsale et les voies spinocérébelleuses et corticospinales (Harding, 2021). Une perte généralisée de la substance blanche du cerveau a également été observée (Harding, 2021). On pense que ces changements pathologiques résultent à la fois d'un développement anormal et d'une dégénérescence progressive (Rezende, 2023).
L'IRM est une technique d'imagerie clé pour suivre la progression de la maladie dans la FRDA. Elle montre une perte de volume dans la substance blanche cérébelleuse, y compris le noyau denté, ainsi que dans d'autres régions, telles que le thalamus, le pons, la moelle, le mésencéphale et les pédoncules cérébelleux supérieurs (Adanyeguh, 2023). Des études IRM longitudinales montrent une atrophie progressive, en particulier dans le cervelet, le thalamus, le diencéphale ventral, le pons et le mésencéphale (Adanyeguh, 2023). En revanche, il a été démontré que le quatrième ventricule augmentait de volume à mesure que ces régions s'atrophiaient.
La DTI a révélé des changements microstructuraux, en particulier dans le cervelet et le tractus corticospinal (Adanyeguh, 2023). L'analyse DTI longitudinale montre une diminution de l'anisotropie fractionnelle (FA) et une augmentation de la diffusivité radiale (RD) dans les pédoncules cérébelleux supérieurs, ainsi qu'une augmentation annuelle de la RD dans les pédoncules cérébelleux inférieurs (Adanyeguh, 2023). Une dégénérescence du tractus dentato-thalamo-cortical (DTT) a également été observée, avec une diminution de l'AF et une augmentation de la diffusivité moyenne (MD) et de la RD, ainsi que des corrélations significatives entre la longueur des répétitions GAA et les métriques DTI, indiquant que les répétitions plus longues sont associées à une dégénérescence plus sévère (Cocozza, 2024).
La MRS a été utilisée pour détecter les changements neurochimiques dans le cervelet et la moelle épinière des patients atteints de FRDA. Les études de MRS ont révélé des altérations des métabolites, telles qu'une diminution du N-acétylaspartate total (tNAA) et une augmentation du myo-inositol (mIns) dans le cervelet, qui ne sont pas visibles avec l'imagerie traditionnelle (Iltis, 2010). Une étude de la moelle épinière a montré une diminution du tNAA et une augmentation du mIns chez les patients FRDA, conduisant à une diminution du rapport tNAA/mIns par rapport aux témoins (Joers, 2022). Les données longitudinales ont également démontré une diminution annuelle de 5.8% de ce rapport. L'ensemble de ces résultats suggère une perte neuronale, une gliose et une myélinisation anormale dans le cerveau et la moelle épinière des patients FRDA (Iltis, 2010; Joers, 2022).
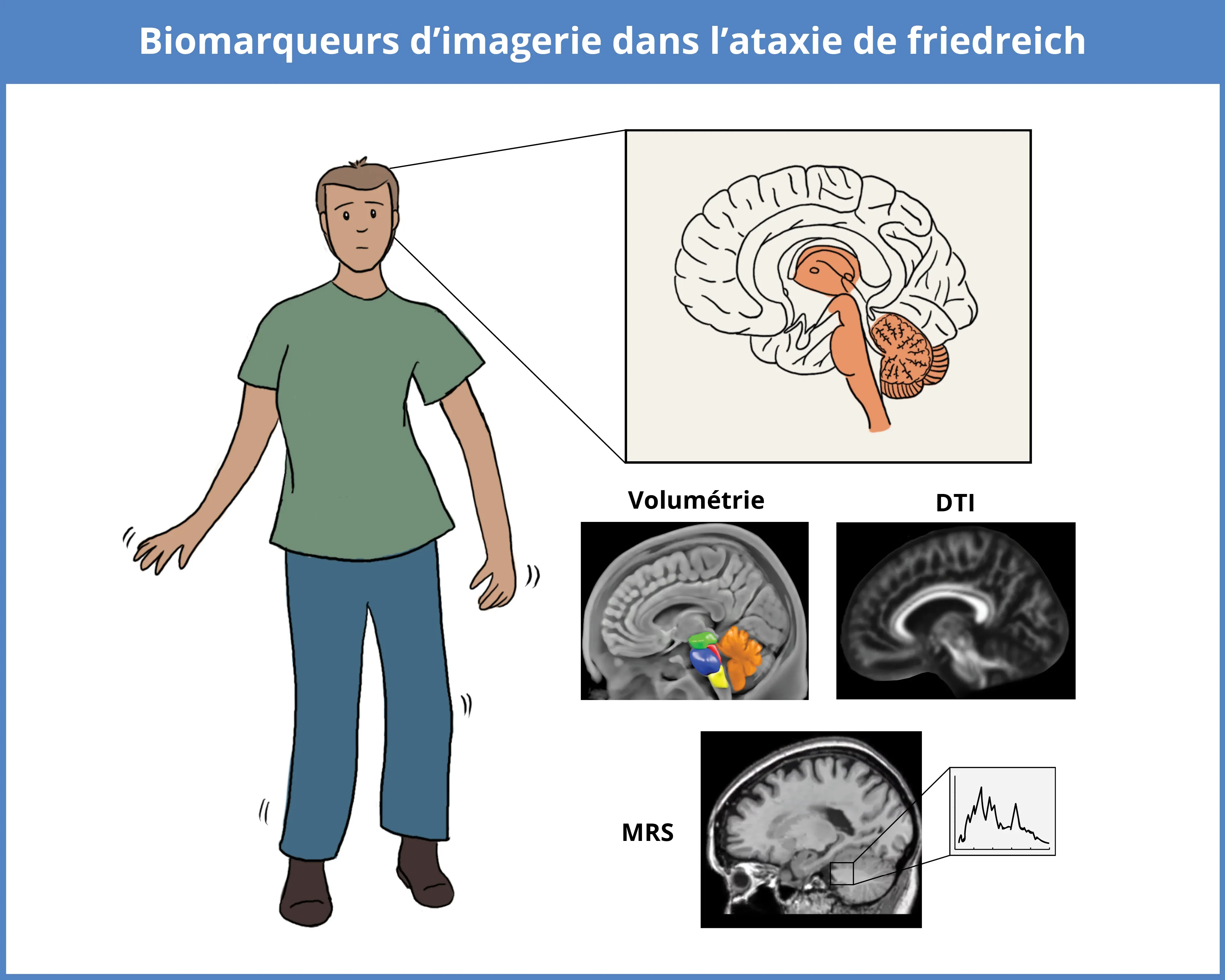
Les biomarqueurs d'imagerie utilisés pour évaluer la FRDA comprennent la volumétrie structurelle basée sur l'IRM pour l'atrophie régionale, la DTI pour les changements microstructurels et la MRS pour les altérations neurochimiques. Ces techniques détectent les changements, en particulier dans le cervelet, le tronc cérébral, le thalamus, le mésencéphale et la moelle épinière.
Les études d'IRM montrent que l'étendue de la neuropathologie dans le FRDA varie selon le stade de la maladie (Harding, 2021). Les données volumétriques de l'IRM suggèrent que des changements dans le noyau denté et le tronc cérébral se produisent au début de la maladie, tandis que la dégénérescence de la matière grise cérébrale devient plus apparente aux stades ultérieurs (Harding, 2021). Ces données d'IRM volumétrique correspondent aux caractéristiques cliniques de la FRDA, où les déficits moteurs prédominent tôt, tandis que les symptômes cognitifs, visuels et auditifs peuvent apparaître plus tard. La progression de la maladie est influencée par la longueur des répétitions GAA, les répétitions plus longues étant liées à une apparition plus précoce et à une progression plus sévère de la maladie. Des études volumétriques indiquent qu'un âge d'apparition précoce est corrélé à une réduction du volume de la substance blanche dans le cervelet, tandis que la diminution des volumes dans le cervelet et le tronc cérébral est négativement corrélée à la durée et à la gravité de la maladie (Harding, 2021).
En résumé, l'IRM et la DTI sont les principales modalités d'imagerie utilisées pour détecter et suivre la progression de la maladie dans la FRDA. Ces techniques fournissent des biomarqueurs fiables pour évaluer les changements structurels et microstructurels dans les principales régions d'intérêt, telles que le noyau denté et la moelle épinière. En outre, la MRS permet de mieux comprendre les changements neurochimiques, en détectant les altérations des métabolites cérébraux. De futurs essais cliniques multicentriques intégrant diverses modalités d'imagerie et stratifiant les participants en fonction de divers facteurs, tels que l'âge d'apparition et le stade de la maladie, permettront de mieux comprendre le FRDA et contribueront au développement de nouvelles thérapies.
Notre équipe se fera un plaisir de répondre à vos questions sur la neuro-imagerie dans l'ataxie de Friedreich et les essais cliniques ou de vous fournir des informations spécifiques sur nos autres services d'imagerie.
Découvrez nos services d'imagerie
Contenu connexe
Informations actualisées sur les meilleures pratiques liées à l'utilisation de la neuroimagerie dans les essais cliniques sur les maladies neurologiques.
Essais cliniques et biomarqueurs d'imagerie pour l'ataxie spinocérébelleuse
Vue d'ensemble des biomarqueurs d'imagerie IRM structurelle, DTI et MRS pour surveiller la progression de la maladie dans les essais cliniques sur l'ataxie spinocérébelleuse.
Biomarqueurs TEP dans les essais cliniques sur la maladie de Huntington
Un aperçu de l'utilisation des biomarqueurs d'imagerie TEP pour les essais cliniques de la maladie de Huntington (MH).
Biomarqueurs de neuro-imagerie pour la sclérose tubéreuse de Bourneville (STB)
Aperçu des biomarqueurs d'IRM et d'imagerie pondérée en diffusion pour évaluer l'efficacité des traitements neurologiques dans les essais cliniques de la STB.
Biomarqueurs IRM dans les essais cliniques de la maladie de Huntington
Un aperçu de l'utilisation des biomarqueurs d'imagerie IRM structurelle et de diffusion pour les essais cliniques de la maladie de Huntington (MH).
Démence frontotemporale (DFT) et atrophie cérébrale par IRM
Biomarqueurs IRM (y compris l'atrophie cérébrale) issus des études FTLDNI sur l'histoire naturelle de la démence frontotemporale (DFT).
L'IRM dans les essais cliniques sur l'atrophie du système multiple (MSA)
Cette ressource donne un aperçu de l'utilité de l'IRM volumétrique et de l'imagerie pondérée en diffusion (DWI) en tant que biomarqueurs dans les études de recherche sur la MSA.